Havuz / Havuz / Getty Images
Temel Çıkarımlar
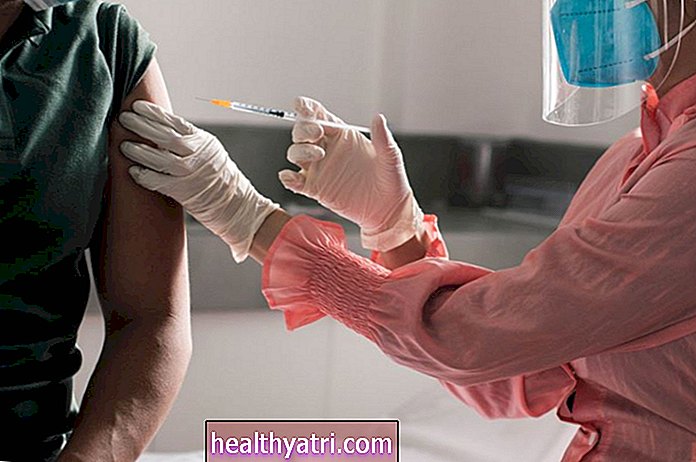
- FDA, Pfizer ve BioNTech tarafından geliştirilen COVID-19 aşısına acil kullanım izni verdi.
- Haber, bir FDA danışma komitesinin, ajansın aşı için yetki vermesini tavsiye etmesinden bir gün sonra geliyor.
- Komite tarafından incelenen veriler, aşıyı% 95 etkili buldu.
- Aşıların dağıtımı, yetkilendirmeden sonraki 24 saat içinde gelebilir.
Gıda ve İlaç Dairesi (FDA), Cuma akşamı ilk COVID-19 aşısına acil kullanım izni verdi. Pfizer Inc. ve Alman BioNTech şirketi tarafından geliştirilen aşı, kısa süre içinde dağıtımına başlayacak.
Haber, Perşembe günü, FDA'nın bir danışma panelinin Pfizer aşısının yetkisi lehine 17-4 oyla bir çekimserle oy verdiği, çok beklenen kamuya açık bir duruşmayı takip ediyor.
Pfizer, 43.000 yetişkin katılımcının yer aldığı klinik araştırmalardan elde edilen verileri sundu.Bu haftanın başlarında, FDA bu verilerin bir kısmını paylaştı, klinik deneyde aşıyı alan kişilerin% 95'inin COVID geliştirmeye devam etmediği gerçeği dahil -19. Enjeksiyon bölgesinde titreme, hafif ağrı ve kızarıklık gibi yan etkiler küçüktü.
Acil kullanım yetkisi (EUA), 16 yaş ve üstü kişiler için geçerlidir. Pfizer ayrıca, 12 yaşından küçük çocuklarda aşının güvenliği ve etkinliği konusunda klinik araştırmalar yürütmektedir ve daha küçük çocuklar için de denemeler eklemesi beklenmektedir.
Daha Fazla Nüfustan Hala İhtiyaç Duyulan Güvenlik ve Etkinlik Verileri
Aşılar ve İlgili Biyolojik Ürünler Danışma Komitesi (VRBPAC) olarak adlandırılan FDA danışma paneli, Pfizer'in aşısının daha fazla popülasyon için güvenli ve etkili olmasını sağlamak için ek önlemler almasını önermektedir. Panel, devam eden klinik araştırmalara daha fazla renkli insanın eklenmesini tavsiye ediyor. Beyaz olmayanların hem COVID-19 kapma hem de virüs yüzünden ölme olasılıkları Beyazlara göre daha yüksek.
Panel ayrıca, daha önce onaylandığı bu hafta Birleşik Krallık'ta aşı alan kişilerde bildirilen iki alerjik reaksiyon vakasını da tartıştı. Philadelphia Çocuk Hastanesi Aşı Eğitim Merkezi direktörü Dr. Paul Offit, Pfizer sunucularına alerjik reaksiyonları sordu ve şiddetli alerjisi olan kişilerin aşıyı almamayı seçebileceklerinden endişelendi. Offit, yaygın alerjisi olan kişilerde aşı konusunda da çalışmalar yapılmasını tavsiye etti.
Birleşik Krallık, bir ilaca veya yiyeceğe karşı anafilaksi öyküsü olan kişilerin aşıyı almamasını tavsiye ediyor. ABD, izne bağlı olarak benzer bir uyarı ekleyebilir. Toplantıdaki FDA çalışanları panele, aşının güvenliği ve etkinliği hakkında tüketiciler için yazılı belgeler üzerinde çalıştıklarını söylediler.
Bu Senin İçin Ne İfade Ediyor
Pfizer'in COVID-19 aşısının yetkilendirilmesi için bir danışma komitesinin tavsiyesine dayanarak, Gıda ve İlaç İdaresi birkaç gün içinde kullanımını onaylayabilir. Dağıtım bundan hemen sonra başlayabilir.Aşının ilk dozlarının sağlık çalışanlarına ve huzurevi sakinlerine uygulanması bekleniyor.
VRBPAC kararının ardından, FDA komiseri Stephen M. Hahn, MD bir açıklama yaptı:
“Normalde, on binlerce kişide incelenen aşıların gözden geçirilmesi süreci aylar sürer. Süreç, bu EUA'nın gözden geçirilmesiyle bağlantılı olarak hızlandırılmış olsa da, FDA'nın uzman inceleme personeli binlerce sayfalık teknik bilgiyi [klinik araştırma verileri dahil], laboratuvarda aşının geliştirilmesine ilişkin klinik olmayan verileri, ve aşının nasıl yapıldığına dair üretim verileri. "
Muhtemelen tüketiciler arasındaki korkuları gidermeye çalışan Hahn, şunları ekledi: “Bu büyük aciliyet döneminde, FDA personeli gözden geçirme süreci boyunca olabildiğince hızlı hareket etme sorumluluğunu hissediyor. Bununla birlikte, kamu sağlığını koruma ve yetkilendirilmiş herhangi bir aşının Amerikan halkının beklediği sıkı güvenlik ve etkinlik standartlarımızı karşılamasını sağlamak için görevlerini yerine getirmeleri gerektiğini biliyorlar. "
Başkan seçilen Joe Biden, komite oylamasından sonra "bilimin bütünlüğü bizi bu noktaya getirdi" şeklinde bir açıklama yaptı.
FDA, aşı dağıtımının yetkilendirmeden sonraki 24 saat içinde gelebileceğini söylüyor.
FDA danışma komitesi, 17 Aralık Perşembe günü Moderna tarafından yapılan ikinci bir COVID-19 aşısını inceleyecek.