Verywell / Vincent Iannelli
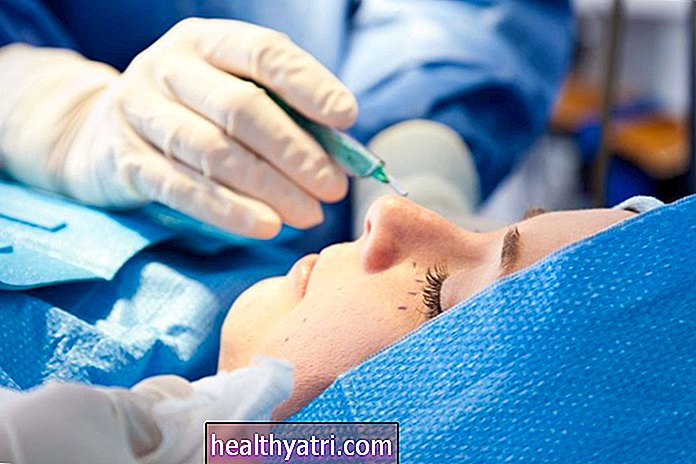
Advair (flutikazon + salmeterol), amfizem ve / veya kronik bronşit dahil olmak üzere astım ve kronik obstrüktif akciğer hastalıklarını (KOAH) tedavi etmek için kullanılan solunan bir ilaçtır.
Advair'e 2003 yılında ABD Gıda ve İlaç Dairesi'nden (FDA) bir kara kutu uyarısı verildi ve salmeterolün yaşamı tehdit eden astım atakları riskini potansiyel olarak artırabileceğini tavsiye etti. Kara kutu uyarısı Aralık 2017'de kaldırıldı. Nedenini öğrenin.
Kara Kutu Uyarılarını Anlama
Kara kutu uyarısı, FDA tarafından halkı bir ilacın ciddi veya yaşamı tehdit eden zarara neden olabileceği konusunda bilgilendirmek için yayınlanan bir önlem ifadesidir. "Kara kutu", kelimenin tam anlamıyla, FDA tavsiyesini içeren ambalaj bilgilerinin üzerinde kalın bir şekilde işlenmiş kutuya atıfta bulunmaktadır.
Kara kutu uyarıları, genellikle ilaç onaylandıktan ve kullanıma sunulduktan sonra yürütülebilecek klinik çalışmaların sonuçları nedeniyle verilir. Bir ilaç onaylandıktan sonra ciddi güvenlik endişeleri ortaya çıkarsa, FDA ambalaj bilgilerinin derhal revize edilmesini isteyecektir. Medya bültenleri de halkı endişeler konusunda uyarmak için dağıtılacaktır.
Advair Hakkında FDA Endişeleri
2003 yılında, Salmeterol Çok Merkezli Astım Araştırma Denemesi (SMART) adlı bir klinik çalışma, salmeterolün astımlı kişilerde, özellikle Afrikalı Amerikalılarda ölüm ve hastaneye yatma riskinde küçük ama önemli bir artışla bağlantılı olduğunu buldu. Bulgular sonucunda Advair dahil salmeterol içeren her türlü ilaçla ilgili kara kutu uyarısı yapıldı.
Çalışma ayrıca, uzun etkili beta agonistleri (LABA) olarak bilinen aynı ilaç sınıfına ait bir ilaç olan formoterol ile benzer bir ölüm ve hastaneye yatma riski bildirdi.
Tek başına kullanıldığında, LABA'lar semptomlarda yeterli rahatlama sağlamaz. Dahası, tek başına kullanılırsa, LABA'lar astım ataklarını tetikleyebilir.
Bu nedenle, ilk önce inhale kortikosteroid (ICS) de içeren Advair gibi birlikte formüle edilmiş ilaçlar yaratıldı.
Bir ICS ile birlikte kullanıldığında, LABA'ların olumsuz etkileri büyük ölçüde azaltılabilir.
Çalışma daha sonra gözden geçirildiğinde, bir ICS ile bir LABA kullanan bireylerin, tek başına bir kortikosteroid kullananlara göre daha fazla veya daha az ölüm veya hastaneye yatma riskine sahip olmadığı ortaya çıktı. Bugün çoğu araştırmacı, SMART denemesinin kötü tasarlandığını ve anormalliği başka türlü açıklayabilecek faktörleri hariç tuttuğunu kabul ediyor.
FDA Bugün Ne Diyor?
2016 yılında, FDA tarafından zorunlu kılınan yeni bir Advair çalışmaları turunun ilki yayınlandı.
AUSTRI çalışması, bazıları 12 yaşından küçük astımlı 11.679 kişide tek başına flutikazon ile kombinasyon salmeterol ve flutikazonun güvenliğini değerlendirdi. ırkla ilgili.
Araştırmacılar, salmeterol-flutikazon alan katılımcılar için astım atakları veya diğer yan etkilerin riskinin, tek başına flutikazon (bir kortikosteroid) alanlara göre daha büyük olmadığını bulmuşlardır.
Çalışma, Advair'in tek bir üründe bir LABA ve kortikosteroid sunarak FDA kara kutu uyarısında önerilen risklerin hiçbirini oluşturmadığını doğruladı.
FDA, tek başına LABA kullanan ürünler için bir kara kutu uyarısını korurken, hem ICS hem de LABA içeren ilaçlar birUyarı ve ÖnlemKullanıcılara LABA'ları kullanmanın risklerini hatırlatmakolmadanbir ICS. Hem ICS hem de LABA içeren ilaçlar, astım ve KOAH tedavisi için FDA onaylıdır.