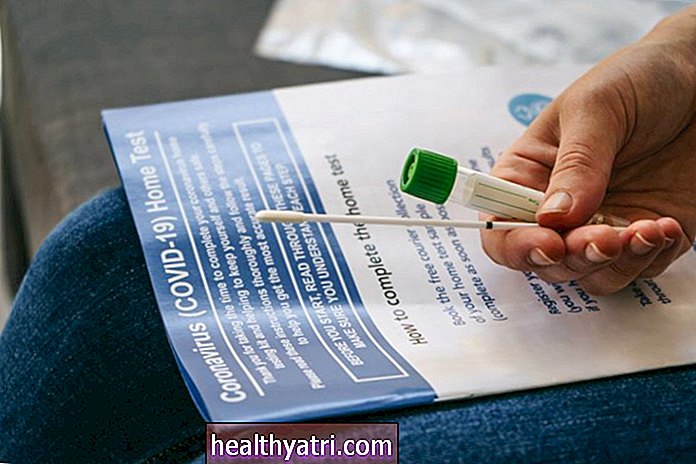
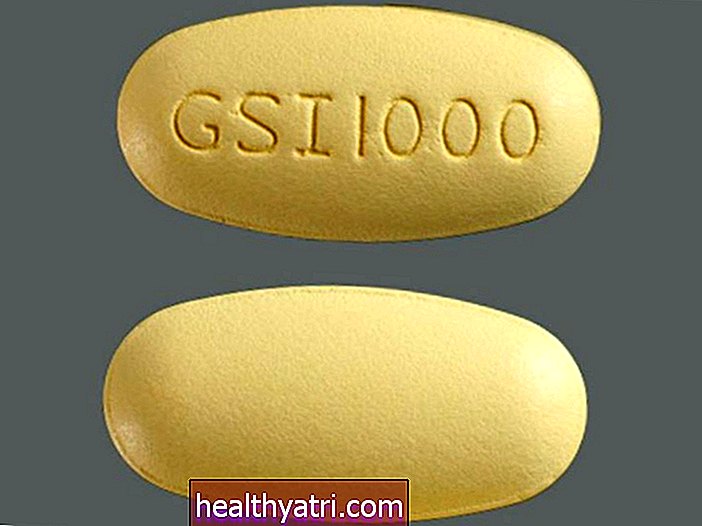
digicomphoto / Getty Images
Temel Çıkarımlar
- Veklury (remdesivir), COVID-19 hastaları için FDA onaylı ilk tedavidir.
- Onay sadece 88 pound'un üzerindeki hastanede yatan hastalarda tedavi içindir.
- Daha önce, ilacın FDA'dan Acil Kullanım İzni vardı.
Gıda ve İlaç Dairesi (FDA) Perşembe günü 12 yaş ve üstü hastanede yatan hastalarda COVID-19 tedavisi için Veklury'yi (remdesivir) onayladı. Bu, COVID-19 için resmi olarak FDA onaylı ilk ilaçtır.
Daha önce, FDA remdesivir için Acil Kullanım İzni (EUA) vermişti, tam onay değil. 1 Mayıs'ta yayınlanan ilk EUA, remdesivir'in ağır COVID-19'u olan hastanede yatan hastalarda kullanılabileceğini söyledi. EUA, 28 Ağustos'ta yeniden yayınlandı ve hastalığın ciddiyetine bakılmaksızın, hastanede yatan yetişkinlere ve COVID-19 vakaları doğrulanmış veya şüpheli çocuklara yaygınlaştırıldı.
İlaç artık onaylanmış olmasına rağmen, onay tüm grupları kapsamamaktadır. Remdesivir almak için hastaların en az 40 kilogram (kg) - yaklaşık 88 pound - ağırlığında olması gerekir. İlk EUA kapsamındaki pediatrik hastalara ilacı sunmaya devam etme çabasıyla, gerektiğinde FDA yeniden yayınladı.bir diğeriHatırlatıcının kullanımı için EUA:
- 3,5 kg ila 40 kg'dan hafif hastanede yatan pediatrik hastalar
- En az 3,5 kg ağırlığında, 12 yaşından küçük hastanede yatan pediyatrik hastalar
FDA Komisyon Üyesi Stephen M. Hahn, yaptığı açıklamada, "FDA, bu benzeri görülmemiş halk sağlığı acil durumu sırasında COVID-19 tedavilerinin geliştirilmesini ve kullanılabilirliğini hızlandırmaya kararlıdır" dedi. "Bugünün onayı, kurumun titizlikle değerlendirdiği ve COVID-19 pandemisinde önemli bir bilimsel kilometre taşını temsil ettiği çok sayıda klinik denemeden elde edilen verilerle destekleniyor. FDA’nın Koronavirüs Tedavi Hızlandırma Programının bir parçası olarak ajans, yeni tıbbi ürünleri hastalara mümkün olan en kısa sürede taşımaya yardımcı olmaya devam ederken, aynı zamanda bunların etkili olup olmadığını ve yararlarının risklerinden daha ağır basıp basmadığını belirleyecektir. "
Remdesivir nedir?
Remdesivir, viral ribonükleik asit (RNA) sentezini inhibe eden doğrudan etkili bir antiviral ilaçtır SARS-CoV-2 dahil koronavirüsler, tek sarmallı RNA genomunun bir ailesidir. Remdesivir'in bu virüslerin çoğalmasını durdurduğu kanıtlanmıştır.
Remdesivir ve COVID-19
Remdesivir, Teksaslı araştırmacılar, sınırlı klinik verilere rağmen, intravenöz ilacı COVID-19 için “en umut verici tedavi” olarak tanımladığında ilk kez manşetlere çıktı.
National Center for Advancing Translational Sciences'da çalışan PhD Matthew D. Sağlık Enstitüleri. COVID-19 Açık Veri Portalı'nın, onaylanan tüm ilaçlar için COVID-19 ile ilgili ilaç yeniden kullanım verilerini ve deneylerini paylaşmasına yardımcı oldu.
Hall Verywell'e "Onaylanmış ilaçların çoğunun ortalama 15 yıl ve birkaç milyar doları geliştirmesi gerekiyor. Ancak 15 yılımız yoktu; 15 haftamız bile olmadı. "
Hall, kendisinin ve ekibinin mevcut kaynakları değerlendirmekle görevlendirildiğini söylüyor.
"Başka hastalıkları tedavi etmek için onaylanmış veya başka hastalıkları tedavi etmek için geliştirilmekte olan, bizim için zaten mevcut olan şeyleri araştırmamız gerekiyordu" diyor. "Henüz onaylanmamış olabilirler, ancak umarım insanlarda olmuşlardır ve güvende olduklarını biliyoruz. Çok sayıda antiviral ilaca sahip olduğumuz için yeterince şanslıyız. Onaylanan ilaçlardan veya ilaç adaylarından remdesivir görünüyor en aktif olanıydı, bu yüzden gerçekten hızlı bir şekilde klinik deneylere geçirilebilir. "
Matthew D.Hall, Doktora
Onaylanan ilaçların çoğunun geliştirilmesi ortalama 15 yıl ve birkaç milyar dolar alır. Ama 15 yılımız yoktu; 15 haftamız bile yoktu.
- Matthew D.Hall, DoktoraFDA başlangıçta 1 Mayıs'ta ağır COVID-19'u olan hastanede yatan yetişkin hastaların remdesivir ile tedavi edilmesine izin vermek için bir EUA verdi. Şiddetli COVID-19'u olan bir kişi şu şekilde tanımlandı:
- Oksijen satürasyonu% 94 veya daha az olan bir hasta
- Ek oksijene ihtiyaç duyan bir hasta
- Mekanik ventilasyon gerektiren bir hasta
- Ekstrakorporeal membran oksijenasyonu gerektiren bir hasta
Genişletilmiş EUA, ilacın daha erken evrelerde veya daha hafif hastalık vakalarında hastalara sunulmasına yardımcı oldu ve onay, yalnızca kullanılabilirliğini artırmalıdır. Hall, hastaların tedavi almak için klinik bir yolun parçası olarak kaydedilmesine gerek olmadığını ve araştırma tesislerinin yakınında yaşamayan kırsal topluluklarda yaşayan insanlara erişimi artırdığını söylüyor.
Hall, "Evde biraz hasta olan kişilerin virüsü vücutlarından daha erken yok etmelerinin daha sonra hastalanmamalarını sağlamak için bir antiviral almalarının iyi olacağına hepimiz hemfikiriz," diyor. Şu anda, remdesivir almak için hastanede olacak kadar hasta olana kadar beklemelisin. Onlara grip için Tamiflu gibi daha önce bir antiviral vererek hastaneye gidecek kadar hasta olmadıklarından emin olmak harika olurdu, (nerede) doktora gidersiniz, hapı alırsınız ve bu sizin zamanınızı kısaltır. hastasın. "
Remdesivir'in gelişimi
Remdesivir başlangıçta Gilead Sciences, ABD Hastalık Kontrol ve Önleme Merkezleri ve ABD Ordusu Bulaşıcı Hastalıklar Tıbbi Araştırma Enstitüsü arasındaki işbirliğinin bir parçası olarak geliştirildi. Batı Afrika Ebola virüsü salgını sırasında ve diğer iki koronavirüs için potansiyel bir terapötik olarak araştırıldı: şiddetli akut solunum sendromu (SARS) ve Orta Doğu solunum sendromu (MERS).
Remdesivir'i Kimler Almalıdır?
Remdesivir'in optimal hasta popülasyonu, dozajı ve tedavi süresi bilinmemektedir. Sağlık hizmeti sağlayıcıları için bir bilgi sayfasında FDA aşağıdaki önerileri sunar:
- 40 kg ve üzeri yetişkinler ve pediyatrik hastalar için önerilen doz, 1. günde 200 mg ve ardından 100 mg'lık dozlardır.
- 3,5 kg ile 40 kg arasında değişen pediyatrik hastalar için önerilen doz, 1. günde 5 mg / kg, ardından sonraki 2.5 mg / kg dozlarıdır.
- İnvaziv mekanik ventilasyon ve / veya ekstrakorporeal membran oksijenasyonu gerektirmeyen hastalar için önerilen toplam tedavi süresi 5 gündür.
- İnvaziv mekanik ventilasyon ve / veya ekstrakorporeal membran oksijenasyonu gerektiren hastalar için önerilen toplam tedavi süresi 10 gündür.
- Bir hasta klinik iyileşme göstermezse, tedavi 10 güne kadar toplam tedavi süresi için 5 güne kadar uzatılabilir.
Gilead Sciences, araştırma amaçlı bir ilaç olarak kabul edilen ve şu anda herhangi bir endikasyon için onaylanmayan remdesivir'in üretimini ve dağıtımını büyütmek için çalışıyor.
Klinik Araştırmalar ve Ön Bulgular
FDA'nın remdesivir'i onaylama kararı, birkaç klinik araştırmadan elde edilen araştırma bulgularına dayanmaktadır ve tıp camiasından karışık görüşlerle karşılanmıştır.
Hall, "Herhangi bir uyuşturucu ya da herhangi bir uyuşturucu adayı hakkında ne düşündüğüm gerçekten önemli değil," dedi. “Gerçekten önemli olan, iyi kontrol edilen bir klinik araştırmadan elde edilen verilerdir. FDA, daha fazla hasta için fayda sağlayacağını düşünmeseydi EUA'nın kapsamını genişletmezdi. "
29 Nisan'da yayınlanan bir çalışmadaNeşter,bir grup doktor ve araştırmacı, Çin'in Hubei kentindeki 10 hastanede şiddetli COVID-19'u olan 237 yetişkin hasta üzerinde randomize, çift kör, plasebo kontrollü bir çalışma yürüttüler ve remdesivir'in iyileşmeyi hızlandırdığını gördüler.
Yazarlar, "İstatistiksel olarak anlamlı olmamakla birlikte, remdesivir alan hastalar, semptom süresi 10 gün veya daha az olan hastalar arasında plasebo alanlara göre sayısal olarak daha hızlı klinik iyileşme süresine sahipti" diye yazıyorlar.
ABD hükümeti tarafından desteklenen bir çalışma, ön bulgularını 22 Mayıs'taNew England Tıp Dergisi1.063 COVID-19 hastasının katıldığı randomize, çift kör, plasebo kontrollü bir çalışmadan. Araştırmacılar, 10 günlük bir remdesivir kürü atananların plaseboya kıyasla daha kısa bir iyileşme süresine sahip olduğunu buldu - medyan 11'e karşı 15 gün.
Yazarlar, "Bu ön bulgular, COVID-19 ile hastaneye yatırılan ve tamamlayıcı oksijen tedavisine ihtiyaç duyan hastalar için remdesivir kullanımını desteklemektedir" diye yazıyorlar. "Bununla birlikte, remdesivir kullanımına rağmen yüksek mortalite göz önüne alındığında, tek başına antiviral bir ilaçla tedavinin muhtemelen yeterli olmayacağı açıktır."
21 Ağustos'taAmerikan Tabipler Birliği DergisiOrta derecede COVID-19 pnömonisi ile hastaneye kaldırılan 584 hastayı içeren randomize bir faz-3 çalışması yayınladı Remdesivir üreticisi Gilead Sciences, Amerika Birleşik Devletleri, Avrupa ve Asya'daki 105 hastanede bu çalışmaya sponsor oldu. Hastalara 5 günlük veya 10 günlük bir remdesivir kürü verildi veya standart bakım verildi. Araştırmacılar, 10 günlük grup arasında sonuçlarda hiçbir fark bulamadı ve 5 günlük grup arasında çok az anlamlı farklılık buldu.
Her üç çalışma da farklı sınırlamalarla karşılaştı ve önemli tasarım farklılıklarına sahipti, bu nedenle elma ile elma karşılaştırması oluşturmak adil değil. Bununla birlikte, klinik araştırmanın ayırt edici özelliği olan bulguların kopyalanması hakkında sorular ortaya çıkarmaktadır.
"Artık hastanede yatan hastalarda farklı sonuçlara sahip üç [randomize kontrol denemesi] var ve bu tutarsızlıkların hasta popülasyonları da dahil olmak üzere çalışma tasarım seçimlerinin eserleri olup olmadığı veya ilacın umulandan daha az etkili olup olmadığı sorusunu gündeme getiriyor. Pittsburgh Tıp Fakültesi araştırmacıları,Amerikan Tabipler Birliği Dergisi21 Ağustos'ta. "Bu nedenle, kalan belirsizlikleri ele almak ve optimal kullanımı bildirmek için tasarlanmış geniş ölçekli randomize kontrol deneylerinde acilen remdesivir ile ilgili daha fazla değerlendirme yapmak akıllıca görünüyor."
Bu Senin İçin Ne İfade Ediyor
ABD Gıda ve İlaç Dairesi ilk COVID-19 tedavi onayını remdesivir'e verdi. Onaylanmış veya şüpheli bir COVID-19 vakasıyla hastaneye kaldırılırsanız, sağlık uzmanınız bu ilacı reçete etmeye karar verebilir.
Remdesivir için Sırada Ne Var?
Gilead Sciences web sitesine göre daha fazla klinik çalışma devam ediyor. Şirket ayrıca, remdesivir'i bir inhaler olarak formüle etmek için geliştirmenin ilk aşamasındadır.
Hall, küresel topluluğun zorluğun üstesinden geldiğini söylüyor, ancak SARS-CoV-2 için bir ilaç arayışı, insan koronavirüsleri için herhangi bir terapötik maddenin bulunmadığı gerçeğiyle birleşti. Son SARS ve MERS salgınları, terapötik maddelerle değil, halk sağlığı önlemleriyle mücadele edildi.
Hall, "Remdesivir ile var olduğu için çok şanslıyız," diyor. "Ebola için geliştirildiği için şanslıyız. Şu anda insanlarda test edilebildiği için şanslıyız. Çünkü remdesivir'i denklemden çıkarırsanız, bundan sonraki en iyi şeyin ne olduğunu bilmiyorum. Yok SARS-CoV-2 enfeksiyonunu tedavi etmek için onaylanmış başka bir ilaç. "